Reparación de Mielomeningocele
Febrero 2016
Reparación fetoscópica versus reparación abierta de Espina Bifida Aperta : revisión sistemática de Outcomes
Luc Joyeux Fetal Diagn Ther Febrero 2016
Background
La espina bífida es el defecto del tubo neural más común y ocurre en 4,9 /
10.000 nacimientos (Registro EUROCAT 2008-2012). En teoría, hay alrededor de
2.600 casos en EEUU- 28 por ańo [1]. En su forma abierta ("aperta" ), la espina
bífida se debe diagnosticar prenatalmente y se presenta como una enfermedad
progresiva [2, 3]. In útero por lo general el deterioro se explica por la
patogenia "2 hits" [4, 5].
En primer lugar, hay falla de cierre del tubo neural a las 6 semanas de gestación. Posteriormente, desde la semana 16 en adelante, hay un dańo secundario a la médula espinal y nervios debido a trauma directo y agentes neurotóxicos en el líquido amniótico, así como tambien en el cerebro , evidenciado por el desarrollo de ventriculomegalia y malformación Chiari II (CM ) [6-9]. Esta último se debe a fuga de líquido espinal cerebral a nivel del defecto, lo que lleva a un "gradiente de succión" [10].
La espina bífida aperta (SBA) es una enfermedad crónica no letal que causa morbilidad significativa; su gravedad depende esencialmente del nivel del defecto [11, 12]. Los nińos pueden tener dificultades en la deambulación debido a déficits sensoriomotores de extremidades inferiores , así como tambien de vejiga, intestino y disfunción sexual [11].
SBA puede causar complicaciones progresivas después del nacimiento, debido principalmente a Chiari II (CM) , hidrocefalia severa que requiera válvula derivativa VP y que causa discapacidades cognitivas llamadas trastornos de aprendizaje y déficit sensoriomotor [11].
El Sindrome de médula espinal anclada es principalmente una complicación en el
sitio de la reparación, que puede causar déficits progresivos y requiere
desanclaje [11, 13]. CM sigue siendo la causa principal de muerte en los
primeros 5 ańos de vida debido a la disfunción de cerebro posterior que se
desarrolla en 17% de los casos de SBA [14].
El estudio randomizado Manejo of de mielomeningocele (MOMS) LINK ha causado un cambio de paradigma en el manejo perinatal de la SBA cuando el diagnóstico se hace a más tardar en el segundo trimestre: MOMS proporcionó evidencia nivel I de que la reparación in útero de la SBA (SAVR), en oposición a reparación posnatal, disminuye la necesidad de derivación ventrículo - peritoneal y mejora los outcomes motores a los 30 meses [15].
Esta técnica consiste en una reparación de capas que se realiza mediante laparotomía materna e histerotomía (acceso abierto : OSBAR) . LINK
OSBAR es una operación muy invasiva con riesgo tanto para la madre como para el feto [15]. Como consecuencia de ello, fueron concebidas las técnicas fetoscópicas para SAVR (FSBAR) con el fin de minimizar la invasividad, disminuir la morbilidad materna, al mismo tiempo que se mantienen los resultados mejorados de los fetos ó neonatos [16].
SAVR clínica se realizó por primera vez por fetocospia en EE.UU.. Sin embargo, fue abandonada rápidamente debido a las limitaciones técnicas y complicaciones graves en una pequeńa serie de casos [16-18]. En Europa, la técnica fue iniciada por Kohl y cols . [19], inicialmente en Bonn (Alemania). Con los ańos, estos cirujanos acumularon una gran experiencia quirúrgica, que publicaron en diferentes reportes [20, 21]. Los outcomes neonatales, según la evaluación independiente por un equipo holandés [22], están disponibles para un número limitado de sus pacientes.
The American College of Obstetrician and Gynecologists Committee Opinion January 2013 Reaffirmed 2015 LINK
A raíz de la publicación del estudio MOMS y trás un entrenamiento intensivo, nuestro equipo decidió ofrecer OSBAR [23, 24]. Como todavía tenemos un interés en la cirugía fetoscópica, el objetivo fue revisar sistemáticamente los resultados de FSBAR [24, 25].
Como punto de referencia se eligieron los resultados obtenidos en el estudio MOMS que debe ser considerado en la actualidad como el estándar de oro para el tratamiento [15].
Fuentes de datos
Estrategia de búsqueda
Se realizó una revisión sistemática en PubMed, Medline (bases de datos NCBI), ISI Web of Science, EMBASE, Scopus y Directorio de Revistas de Acceso Abierto. Además, se incluyó una búsqueda de literatura (Google Académico) hasta septiembre de 2015. Los términos (free text y MeSH) utilizados para la búsqueda fueron
"spinal
dysraphism", "spina bifida (cystica)" ó "myelomeningocele" combinado con "f(o)etoscopy"
ó "f(o)etal therapy", así como nombres de
autores principales de un programa de SAVR fetal. Esta revisión sistemática se
ha registrado en registro PROSPERO (CRD 42015017172; 6 de abril de de 2015).
El Outcome Primario fue mortalidad perinatal, es decir, número de muertes
fetales y
postnatal (dentro de 28 días de vida) . Los Outcomes secundarios
fueron outcomes operatorio, materno, fetal, neonatal e infantil. Los
reportes se clasificaron ya sea como
estudios sobre experiencia temprana (≤ 30 casos), un punto de corte propuesto por Kohl
[26, 27] ó más allá de ese punto (referidos como experiencia "más tardía" ). Los
casos reportados como abstracts , reportes de casos individuales, duplicados ó
reportes que carecen de la mayoría de datos de resultados obstétricos y
/ o después del parto, fueron excluídos.
Se evaluó la calidad (buena, regular y mala) y el riesgo de sesgo de los estudios elegibles usando criterios adaptados descritos en el Manual Cochrane para Revisiones Sistemáticas de Intervenciones y la herramienta de evaluación de la calidad del estudio de American National Institutes of Health [28–30]
Análisis estadístico
Se clasificaron los estudios basados en el número de procedimientos realizados por el equipo, ya sea como experiencia temprana ó experiencia más tardía (estudios con > 30 pacientes) . Los valores de p < 0,05 se consideraron estadísticamente significativos.
Resultados
Descripción de estudios
Nuestra búsqueda bibliográfica identificó 16 publicaciones (Figura 1). La selección según criterios de elegibilidad dejó 12 estudios elegibles para su posterior evaluación de texto completo, después de lo cual se excluyeron 7 informes. Dos reportes de casos de Bruner y cols [16, 18] que describen los mismos pacientes (n = 4) y 1 reporte de caso de Farmer y cols. [17] (n = 3) de dos equipos Americanos fueron excluídos debido a datos incompletos. Estos grupos más tarde abandonaron su programa FSBAR y se cambiaron a OSBAR debido a una combinación de fallas técnicas, complicaciones y muerte fetal. Dos reportes de casos y series de casos 1 (n = 2, 3 y 16, respectivamente) de Kohl y cols . [19-21] fueron excluidos debido a que los datos eran incompletos y reportados en un artículo posterior (n = 19) [22]. Un reporte de caso de Pedreira et al. [36] también se excluyó ya que todos los casos habían sido incluídos en un estudio posterior más completo.
Esto dejó en total 5
series de casos de 2 programas para evaluación (Figura
1). Desde el primer programa (Kohl
y cols, Alemania), se incluyeron pacientes de 4 reportes que se superponen: 1
publicado en 2012 (n = 19), 2 en 2014 (n = 51) y 1 reporte final en 2015 (n =
71) [ 22, 26, 27, 35]. La quinta series (n = 10) procedía de Pedreira
y cols [37] (Sao Paulo, Brasil).
Figura 1.- Estudio de diagrama de flujo adaptado a partir del diagrama de flujo de PRISMA 2009 [61].
Calidad y riesgo de sesgo en estudios incluídos
Grivell y cols [38] demostraron
recientemente que el estudio MOMS era de alta calidad con bajo riesgo de
sesgos.
Del grupo de Kohl, el estudio de casos y controles por Verbeek y cols. [22]
(2012, n = 19) representa un reporte de buena calidad por parte de evaluadores
independientes (tabla 1). Sin embargo,
tienen un sesgo de deserción
alta, ya que los resultados neonatales e infantiles faltan [26, 27].
Los datos de la serie de casos de Pedreira y cols [37] son de buena calidad (tabla 1). Los outcomes después de 12 meses no están disponibles todavía (tabla 2).
Efectos de las intervenciones
La Tabla 2 muestra la heterogeneidad clínica y metodológica entre la experiencia temprana y más tardía con FSBAR. Existe una heterogeneidad importante en términos de selección de pacientes. En cuanto a la experiencia temprana de Kohl en 30 pacientes operados en Bonn (Alemania; 2003 a junio de 2010), solo se reportaron 19 pacientes consecutivos (2003-2009) [22]. Pedreira et al. [34, 36] solamente operaron pacientes de SBA lumbosacra y la mayoría de los pacientes (7/10) fueron operados después de 26 semanas de gestación. Esto difiere de los criterios utilizados en estudio MOMS con operación entre 19.0 y 25.9 semanas de gestación [15]. Los reportes de experiencia más tardía del grupo de Kohl tienen heterogeneidad similar.
Tres papers consecutivos informan
sobre los pacientes operados en Giessen (Alemania) entre julio de 2010 y junio
de 2013, pero no cubren totalmente la misma cohorte. Dos papers (2014) tratan
de los outcomes operatiro, resultados maternos y fetales de 51 madres que se
sometieron a FSBAR [26, 27] y tercer paper (2015) sobre la mortalidad
infantil y resultados neurológicos postnatales al 1 ańo de vida en 71
fetos sometidos con éxito a FSBAR [35].
Tabla 1. Evaluación de la Calidad de los estudios elegibles mediante los criterios descritos en el Manual Cochrane para Revisiones Sistemáticas de Intervenciones y la herramienta de evaluación de la calidad del American National Institutes of Health (NIH) [28 – 30]
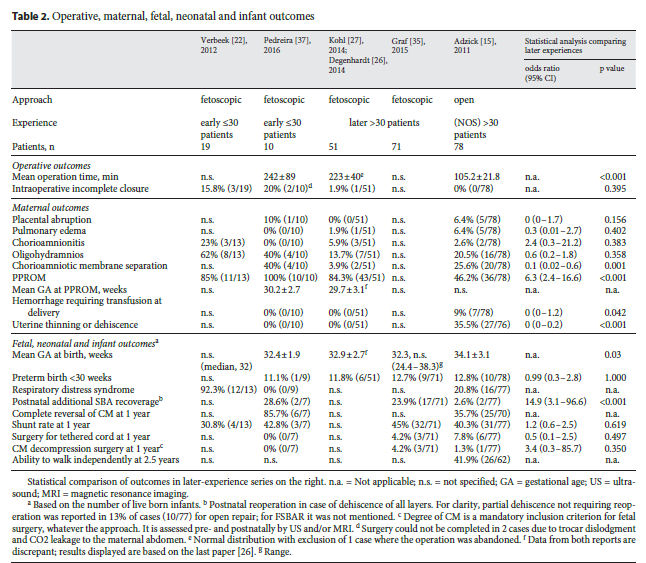
Debido a la heterogeneidad entre los estudios que informan sobre fetoscopía temprana y experiencia posterior, estos datos no se pudieron combinar impidiendo hacer un meta-análisis para su posterior comparación con los datos del estudio MOMS. Por lo tanto, se restringió el análisis estadístico al grupo de experiencia más tardía , es decir, los resultados de 51 pacientes (outcomes operatorios, materno y fetal) y 71 pacientes (outcomes de mortalidad infantil y neurológicos postnatales a los 12 meses) reportados por el grupo de Kohl [26, 27 , 35] en comparación con 78 pacientes del estudio MOMS [15] (Tabla 2).
Tabla 2.- Operative, maternal, fetal, neonatal and infant outcomes

Outcome primario
La mortalidad perinatal fue mayor en la experiencia inicial de FSBAR. En la experiencia posterior (> 30 pacientes), sin embargo, la mortalidad perinatal era comparable a la cirugía abierta (5,9 versus 2,6%, p = 0,258 ; Tabla 3).
Tabla 3.- Mortality rate for FSBAR with statistical analysis for comparison of later-experience fetoscopic studies to OSBAR
Outcomes secundarios
Técnica quirúrgica.
En la descripción del método, tanto la
técnica FSBAR [27, 36, 37] como la técnica OSBAR [15] describen técnicas de disección circunferencial
de la placoda neural del tejido circundante, con eliminación de todos
los elementos epiteliales patológicos. Sin embargo, no está claro si se realiza un desanclaje completo en el enfoque fetoscópico, mientras que para el
enfoque abierto se especifica que se permite que la placoda caiga en el canal
espinal [15, 39]. La técnica de cierre difiere entre las técnicas de fetoscopía
del grupo de Kohl y el grupo de Pedreira. Además, los enfoques de fetoscopía y
abiertos son técnicamente diferentes (Tabla 4).
OSBAR se realiza con más frecuencia con 2 capas (duramadre y piel) y sin
parche. Si no hay suficiente duramadre para el cierre, se utiliza un parche DuraGen ® como sustituto; si no es posible obtener el cierre primario de la
piel, se hacen incisiones relajantes ó se utiliza un parche Alloderm ® [15]. Pedreira y colegas [40-42] describen un cierre fetoscópico de
2 capas
estandarizado, que consiste en un parche de celulosa subcutánea que es
cubierto por piel y actúa como un andamio ó matriz para la duramadre, ampliamente
probado en modelos animales. La técnica de cierre en grupo de Kohl
ha evolucionado con el tiempo. En la experiencia inicial (≤ 30 casos), el cierre
consistió en una doble capa de parches (Durasis® parche de fascia cubierto
por una Gore ® Preclude ® parche para la piel de membrana pericárdica ) ó
una sola capa de Gore ® Preclude ® parche para la piel [20-22 ].
En la experiencia más tardía en 51 procedimientos FSBAR, a excepción de 1 con cierre incompleto, la reparación consistió en ya sea una sola capa de Surgisis ® parche de piel (n = 30/50, es decir, 60%), una capa doble de Surgisis ® parche para piel cubierto por Gore ® Preclude ® parche para piel (n = 14/50, es decir, 28%), o una triple capa de Surgisis ® parche para piel cubierta por dos parches de piel Gore ® Preclude ® (n = 2/50, es decir, 4%), una doble capa de Surgisis parche fascia cubierto por la piel (n = 2/50, es decir, 4%) ó una sola capa de piel normal (2/50, es decir, 4%) [26, 27].
Finalmente, en el estudio
más tardío sobre 71 FSBAR, el cierre consistió en una sola capa de parche
para piel Surgisis ® (48/71, es decir, el 67,6% de los casos), una capa doble
ó triple de
parche para piel Surgisis ® cubierto por 1-2 Gore parches cutáneos
de Gore ® Preclude ®
(21/71, es decir, 29,6%) ó una sola capa de piel normal (2/71, es
decir, 2,8%) [35].
En resumen, el grupo alemán en sus 3 últimas publicaciones describe cierre en una sola capa piel aumentado con parche Surgisis ® después de socavar la lesión como la técnica más comúnmente realizado en 30/50 (60%) [26, 27] y 48 / 71 (67,6%) de los pacientes [35] ( Tabla 4).
De lo anterior, debe quedar claro que FSBAR en realidad sería descrito con más precisión como cobertura fetoscópica con parche de la SBA.
Tabla 4.- Comparación de técnicas quirúrgicas
Outcomes operatorios.
Tanto en la experiencia inicial ó temprana de Pedreira y Kohl y la experiencia posterior ó tardía de Kohl, la FBAR requiere el doble del tiempo operatorio que el de la OSBAR de referencia (223 ± 40 versus 105,2 ± 21,8 min, p < 0,001). La tasa de cierre incompleto era tan alto como 15,8 a 20% en las primeras experiencias.
Sin embargo, con un mayor número de casos, el cierre incompleto del defecto era tan frecuente en FSBAR como en OSBAR (1,9 versus 0 %, p = 0,395; Tabla 2).
Outcomes maternos y fetales.
En las primeras experiencias de FSBAR, las tasas de corioamnionitis, oligohidramnios, rotura prematura de membranas, prematuridad, procedimientos quirúrgicos postnatales adicionales y síndrome de dificultad respiratoria fueron mayores en comparación con los datos del MOMS . La tasa de shunt ó válvula derivativa al 1 ańo fue comparable (30,8 - 42,8 versus 40,1%). Debido a datos incompletos, no se pudo obtener conclusiones sobre los siguientes resultados : tiempo operatorio, desprendimiento de placenta, edema pulmonar, separación de membranas corioamnióticas, edad gestacional promedio al momento de rotura prematura de membranas, hemorragia que requiere transfusión en el parto, adelgazamiento ó dehiscencia uterino, reprotección posnatal adicional de la SBA , inversión completa de CM (Chiari II) a 1 ańo, cirugía de médula anclada a 1 ańo y capacidad de caminar de forma independiente a los 2,5 ańos (tabla 2).
En la experiencia posterior, FSBAR se asoció con el doble de tasa de rotura prematura de membranas (84 versus 46%, p < 0,001), con edad gestacional al nacer más baja (32,9 versus 34,1 semanas, p = 0,03) y necesidad 10 veces mayor de necesidad adicional de cirugía postnatal de SBA (28 v ersus 2,56%, p < 0,001).
No hubo diferencias en la tasa de oligohidramnios, edema pulmonar, desprendimiento de placenta y corioamnionitis, ni hubo diferencia en la necesidad de válvula derivativa, desanclaje de médula ó descompresión de CM (Chiari) a los 12 meses. FSBAR se asoció con menor tasa de hemorragia que requiere transfusión al parto (0 versus 9%, p = 0,042), tasa 6 veces menor de separación de membrana corioamnióticas (4 versus 26%, p = 0,001) y ausencia total de adelgazamiento de la cicatriz uterina o dehiscencia (0 versus 36%, p < 0,001). Dada la ausencia de ciertos resultados postnatales para FSBAR (síndrome de dificultad respiratoria, inversión completa de CM a 1 ańo y la capacidad de caminar de forma independiente a los 2,5 ańos), no se pudo efectuar una comparación para estos parámetros (tabla 2).
Discusión
El objetivo de esta revisión sistemática
fue comparar las técnicas quirúrgicas y los outcomes ó resultados de FSBAR con OSBAR. Se
concluye que después de 30 casos FSBAR : 1) es técnicamente diferente de OSBAR 2) tiene
mortalidad perinatal , tasa de cierre incompleto intraoperatoria, tasa de desprendimiento de placenta, tasa de edema
pulmonar, tasa de corioamnionitis, tasa de oligohidramnios,
vávula derivación ó desanclaje de médula ó tasa de descompresión CM a los 12 meses
comparables 3)
tiene un tiempo operatorio más largo, doble de tasa de rotura
prematura de membranas, edad gestacional más precoz al nacer,
necesidad 10 veces
mayor de cirugía adicional para SBA posnatal 4) tiene una tasa 6 veces
inferior de separación de membrana corioamniótica y ausencia de hemorragia que
requiere transfusión en el parto y de adelgazamiento ó dehiscencia uterina.
Los
outcomesó resultados neonatales, inversión completa de CM a 1 ańo y outcomes
funcionales neurológicos a los en 2.5 ańos para FSBAR todavía no están disponibles;
por lo tanto, no pueden hacerse comparaciones. Al compilar los datos de FSBAR,
los autores discriminaron entre las experiencias de los operadores temprana y tardía
dado que se describen la experiencia temprana y la experiencia posterior.
Incluso si no se había asignado una curva de aprendizaje de manera objetiva, se utilizó un punto de corte de 30 casos, según lo sugerido por Kohl et
al. [27], un número que también se cita para otras cirugías fetoscópica como
el láser [43], o para procedimientos laparoscópicos complejos [44-47]. De hecho,
la mortalidad perinatal, tasa de cierre incompleto intraoperatoria y la tasa de
válvula de derivación a los 12 meses fue comparable a OSBAR después de 30 casos.
Tanto para las experiencias tempranas y
tardías, se observó un riesgo significativo para sesgo de inconsistencia y
deserción. Para la experiencia inicial hay sólo 1 informe sobre 13/19
pacientes que fueron evaluados neurológicamente a 1 ańo por un evaluador
independiente, sin embargo, los resultados comparables en los demás pacientes
operados durante el mismo período de tiempo fueron a nuestro conocimiento no
publicado [22] . Por lo tanto, sólo el estudio de Brasil ofrece un conjunto
completo de datos sobre experiencia temprana [37]. Para la experiencia más
tardía se observó una diferencia de al menos 20 pacientes en los siguientes
reportes del grupo de Kohl [26, 27, 35], a pesar de que cubren el mismo período de
tiempo.
Hemos observado que ambos enfoques , fetoscópico y abierto producen neuroprotección comparable a corto plazo, a
pesar de diferencias bastante grandes en la técnica operatoria. Esto es
destacable
y a menudo pasa desapercibido. Mientras que la mayoría de los procedimientos
abiertos se hacen de una manera muy similar a lo que se hace durante el
procedimiento postnatal, es decir, disección de placoda neural y cierre
del defecto en 2 ó 3 capas, la descripción de FSBAR es menos clara con
respecto a la extensión del desanclaje de la médula espinal. FSBAR también
sustituye sistemáticamente el cierre por planos mediante la reparación aumentada
con parches
de la duramadre y / o la piel.
Durante OSBAR, el uso de aumento de parche se
limita a pacientes con duramadre insuficiente para el cierre y / o cuando no es
posible obtener cierre de la piel [15]. Sorprendentemente, esta
diferencia en la técnica no parece impactar algunos outcomes ó resultados neurológicos a corto
plazo, como lo demuestran los números comparables de procedimientos de
descompresión para CM (Chiari) y derivación (válvula derivativa).
Como consecuencia de la diferencia en la
técnica, el cierre incompleto del defecto no se produjo prenatalmente después de
OSBAR en oposición a FSBAR. A pesar de ello, la tasa de cierre incompleto
intraoperatoria no fue significativamente mayor después de FSBAR. Este último
también conduce a una mayor necesidad de procedimientos postnatales adicionales
a nivel de la lesión. En un resumen sobre su experiencia
tardía, el grupo alemán reportó una tasa de reprotección postnatal de hasta
40% (n = 33) [33]. En la última serie de casos, se requirió reoperación en 24%
debido a fugas de líquido cerebral espinal (41%), cierre incompleto (29,5%) ó defecto de piel (29,5%) [35].
Inicialmente frecuente (15,8-20%), sin embargo, más adelante en muy raras ocasiones (1,9%), el procedimiento in útero tuvo que ser abandonado prematuramente, dejando la reparación neuroquirúrgica incompleta. Las razones pueden ser factores maternos como obesidad, pero también otras limitaciones técnicas tales como el tamańo del defecto, posición fetal subóptima y una placenta anterior.
Otro parámetro clínicamente relevante es la necesidad de desanclaje posnatal después de completar SAVR in útero. En los pacientes con SBA reparada postnatalmente, el síndrome de médula anclada ocurre en 78-100% de los casos. Por lo general, es un efecto secundario de la formación de tejido cicatricial en el sitio quirúrgico y aproximadamente 20-50% de los nińos con el tiempo requerirá desanclaje quirúrgica [11, 13, 49]. Si la OSBAR prenatal aumenta la necesidad de desanclaje siempre ha sido un tema de debate, pero en estudio MOMS no fue reconocido a mediano plazo [15]. En esta revisión, la cirugía para médula anclada al 1 ańo después FSBAR era comparable a la de OSBAR.
Hay un efecto sorprendente de aumento de la experiencia que causa disminución de los efectos secundarios. La experiencia inicial en FSBAR [22, 37] fue asociada con mayores tasas de mortalidad, oligohidramnios, rotura prematura de membranas y prematuridad cuando se compara con experiencia OSBAR más tardía (tabla 2). La razón de la persistencia de altas tasas de rotura prematura de membranas sigue sin estar clara. Parece tentador relacionar ésta con la necesidad de múltiples trócares. También el tamańo de los sitios de punción puede jugar un papel. Los puertos tienen un diámetro exterior de 4 (12 Fr), 5 ó 5.3 (16 Fr) mm, sin embargo, sus defectos de membrana después del parto varían de 20 a 100 mm de diámetro [36]. Esto había sido observado anteriormente para procedimientos de punción única [54]. Otros factores podrían desempeńar un papel : uso de insuflación de CO2, procedimiento largo y abordaje percutáneo. Se requiere al menos 3 trócares en el útero que someten al útero y membranas amnióticas a fuerzas de cizallamiento significativas cuando los instrumentos son manipulados.
Si este problema se resuelve ya sea por mejores técnicas de cierre [27, 36, 55] ó reduciendo el número de trocares tendrá que ser demostrado. Mientras tanto, PROM - y subsiguiente prematuridad - sigue siendo el talón de Aquiles de la cirugía fetoscópica [56]. De todos modos, todas las diferencias técnicas anteriores, así como los diferentes resultados para cada parámetro específico deben impulsar cuidado al comparar los resultados. Hay un beneficio muy relevante de FSBAR, que no puede ser ignorado. Desde un punto de vista de la madre, aparte de invasividad menor al momento del procedimiento, no se observó adelgazamiento o dehiscencia a nivel de las inserciones de los puerto al momento del parto. Esto podría significar que el útero está menos comprometido en el embarazo actual así como tambien en embarazos futuros, acortando potencialmente el intervalo entre embarazos.
Sin embargo, las determinaciones de adelgazamiento ó dehiscencia uterino fueron subjetivas y no definidas a priori en cualquiera de las técnicas. En ausencia de complicaciones, el modo de parto ha sido por cesárea a las 37 semanas siguiendo a OSBAR (segmento uterino inferior) versus 39 semanas después de FSBAR . No se ha asignado aún relevancia clínica a este hallazgo uterino, sin recomendaciones publicadas para futuros embarazos más allá de cesárea para cirugía fetal abierta. A las madres se les recomienda actualmente retrasar la concepción durante 18-24 meses y en los embarazos posteriores tener parto a las 36 semanas por cesárea antes del inicio del trabajo de parto [57]. El seguimiento a largo plazo no ha mostrado ninguna diferencia en la fertilidad materna posterior [57, 58].
Existen varias limitaciones para esta revisión sistemática. Esto es principalmente debido al sesgo analítico potencial en el proceso de revisión. En primer lugar, esta revisión se refiere, finalmente, a sólo 3 reportes de un grupo alemán con suficiente experiencia con FSBAR. En segundo lugar, los criterios de inclusión para cirugía fetal varían entre los grupos, aunque CM (Chiari) es obligatorio independientemente del enfoque. En el estudio MOMS , la reparación se limitó entre 19 y 26 semanas debido a que la eficacia de procedimientos más tardíos no ha sido demostrada [59, 60]. Para FSBAR, el equipo brasileńo operó entre 25 y 28 semanas, con 70% de los pacientes operados después de 26 semanas [34, 36]. Si bien es cierto que los efectos de una operación más tardía son mínimos o inexistentes, los resultados reportados más arriba del grupo de Brasil son en realidad una subestimación del efecto.
El
equipo alemán realizó las operaciones hasta 29 semanas de gestación, sin
embargo, la gran mayoría (67/71 pacientes) fueron operados antes de las 26
semanas [26, 27, 35]. Por lo tanto, se supone que el efecto observado
actualmente es representativo de lo que se puede esperar. Por último, al
comparar la necesidad de derivación valvular , se debe llegar a una conclusión cautelosa
dado que los numerosos criterios para colocación de válvula derivativa difieren
entre todas las instituciones FSBAR y OSBAR.
En conclusión, FSBAR multitrócar es técnicamente diferente de su alternativa abierta. Aceptando las muchas limitaciones para una comparación adecuada, los autores concluyen que después de una curva de aprendizaje inicial, FSBAR aumenta el riesgo de rotura prematura de membranas y parto prematuro. Además el tiempo operatorio es mucho más largo que con cirugía abierta, pero las consecuencias clínicas de este hallazgo no están todavía claras dado que el feto permanece en un ambiente cálido y líquido. FSBAR decididamente disminuye la morbilidad materna y evita los problemas inherentes a la cicatriz uterina por histerotomía.
La mortalidad perioperatoria es comparable, así como los outcomes a los 12 meses, a excepción de inversión completa de CM que no se reportó. Se requerirán los resultados a largo plazo, tanto para evaluar la médula, así como la función cerebral. En ausencia de datos convincentes, podemos esperar continua controversia sobre si ambos procedimientos son igualmente efectivos. Idealmente, se requiere una comparación de ambos enfoques en un estudio controlado randomizado de tamańo adecuado. Dada la experiencia multicéntrica con ambos procedimientos, ésto representa un enorme desafío, a menos que se acuerde un diseńo alternativo. Los datos prospectivos en un registro internacional dedicado podría ofrecer una alternativa válida para comparar los diferentes enfoques. Mientras tanto, parece prudente considerar FSBAR un procedimiento en investigación. También parece prudente insistir en una mayor investigación traslacional, en especial para investigar si las reparaciones con parches son tan eficaces como las reparaciones en capas. Por otra parte, una inversión de traslación rigurosa en el progreso tecnológico puede hacer a la reparación fetoscópica más eficaz y menos traumática para las membranas.
Referencias
Garne E, Dolk H, Loane M, Boyd PA: EUROCAT website data on prenatal detection rates of congenital anomalies. J Med Screen 2010; 17: 97–98.
Coleman BG, Langer JE, Horii SC: The diagnostic features of spina bifida: the role of ultrasound. Fetal Diagn Ther 2015; 37: 179–196.
Mirsky DM, Schwartz ES, Zarnow DM: Diagnostic features of myelomeningocele: the role of ultrafast fetal MRI. Fetal Diagn Ther 2015; 37: 219–225.
Heffez DS, Aryanpur J, Hutchins GM, Freeman JM: The paralysis associated with myelomeningocele: clinical and experimental data implicating a preventable spinal cord injury. Neurosurgery 1990; 26: 987–992.
Meuli M, Meuli-Simmen C, Hutchins GM, Yingling CD, Hoffman KM, Harrison MR, Adzick NS: In utero surgery rescues neurological function at birth in sheep with spina bifida. Nat Med 1995; 1: 342–347.
Korenromp MJ, van Gool JD, Bruinese HW, Kriek R: Early fetal leg movements in myelomeningocele. Lancet 1986; 1: 917–918.
Sival DA, Begeer JH, Staal-Schreinemachers AL, Vos-Niel JM, Beekhuis JR, Prechtl HF: Perinatal motor behaviour and neurological outcome in spina bifida aperta. Early Hum Dev 1997; 50: 27–37.
Sival DA, Guerra M, den Dunnen WF, Batiz LF, Alvial G, Castaneyra-Perdomo A, Rodriguez EM: Neuroependymal denudation is in progress in full-term human foetal spina bifida aperta. Brain Pathol 2011; 21: 163–179.
Stiefel D, Copp AJ, Meuli M: Fetal spina bifida in a mouse model: loss of neural function in utero. J Neurosurg 2007; 106: 213–221.
McLone DG, Dias MS: The Chiari II malformation: cause and impact. Childs Nerv Syst 2003; 19: 540–550.
Mitchell LE, Adzick NS, Melchionne J, Pasquariello PS, Sutton LN, Whitehead AS: Spina bifida. Lancet 2004; 364: 1885–1895.
Rintoul NE, Sutton LN, Hubbard AM, Cohen B, Melchionni J, Pasquariello PS, Adzick NS: A new look at myelomeningoceles: functional level, vertebral level, shunting, and the implications for fetal intervention. Pediatrics 2002; 109: 409–413.
Stiefel D, Shibata T, Meuli M, Duffy PG, Copp AJ: Tethering of the spinal cord in mouse fetuses and neonates with spina bifida. J Neurosurg 2003; 99: 206–213.
Worley G, Schuster JM, Oakes WJ: Survival at 5 years of a cohort of newborn infants with myelomeningocele. Dev Med Child Neurol 1996; 38: 816–822.
Adzick NS, Thom EA, Spong CY, Brock JW, Burrows PK, Johnson MP, Howell LJ, Farrell JA, Dabrowiak ME, Sutton LN, Gupta N, Tulipan NB, D’Alton ME, Farmer DL: A randomized trial of prenatal versus postnatal repair of myelomeningocele. N Engl J Med 2011; 364: 993–1004.
Bruner JP, Richards WO, Tulipan NB, Arney TL: Endoscopic coverage of fetal myelomeningocele in utero. Am J Obstet Gynecol 1999; 180: 153–158.
Farmer DL, von Koch CS, Peacock WJ, Danielpour M, Gupta N, Lee H, Harrison MR: In utero repair of myelomeningocele: experimental pathophysiology, initial clinical experience, and outcomes. Arch Surg 2003; 138: 872–878.
Bruner JP, Tulipan NB, Richards WO, Walsh WF, Boehm FH, Vrabcak EK: In utero repair of myelomeningocele: a comparison of endoscopy and hysterotomy. Fetal Diagn Ther 2000; 15: 83–88.
Kohl T, Hering R, Heep A, Schaller C, Meyer B, Greive C, Bizjak G, Buller T, Van de Vondel P, Gogarten W, Bartmann P, Knopfle G, Gembruch U: Percutaneous fetoscopic patch coverage of spina bifida aperta in the human – early clinical experience and potential. Fetal Diagn Ther 2006; 21: 185–193.
Kohl T, Tchatcheva K, Merz W, Wartenberg HC, Heep A, Muller A, Franz A, Stressig R, Willinek W, Gembruch U: Percutaneous fetoscopic patch closure of human spina bifida aperta: advances in fetal surgical techniques may obviate the need for early postnatal neurosurgical intervention. Surg Endosc 2009; 23: 890– 895.
Kohl T, Tchatcheva K, Weinbach J, Hering R, Kozlowski P, Stressig R, Gembruch U: Partial amniotic carbon dioxide insufflation (PACI) during minimally invasive fetoscopic surgery: early clinical experience in humans. Surg Endosc 2010; 24: 432–444.
Verbeek RJ, Heep A, Maurits NM, Cremer R, Hoving EW, Brouwer OF, van der Hoeven JH, Sival DA: Fetal endoscopic myelomeningocele closure preserves segmental neurological function. Dev Med Child Neurol 2012; 54: 15–22.
Endo M, Van Mieghem T, Eixarch E, De Coppi P, Naulaers G, Van Calenbergh F, De Catte L, Devlieger R, Lewi L, Eggink A, Nicolaides K, Gratacos E, Deprest J: The prenatal management of neural tube defects: time for a reappraisal. Fetal Matern Med Rev 2012; 23: 158–186.
Ovaere C, Eggink A, Richter J, Cohen-Overbeek TE, Van Calenbergh F, Jansen K, Oepkes D, Devlieger R, De Catte L, Deprest JA: Prenatal diagnosis and patient preferences in patients with neural tube defects around the advent of fetal surgery in Belgium and Holland. Fetal Diagn Ther 2015; 37: 226–234.
Deprest JA, Flake AW, Gratacos E, Ville Y, Hecher K, Nicolaides K, Johnson MP, Luks FI, Adzick NS, Harrison MR: The making of fetal surgery. Prenat Diagn 2010; 30: 653– 667.
Degenhardt J, Schurg R, Winarno A, Oehmke F, Khaleeva A, Kawecki A, Enzensberger C, Tinneberg HR, Faas D, Ehrhardt H, Axt- Fliedner R, Kohl T: Percutaneous minimallyinvasive fetoscopic surgery for spina bifida aperta. II. Maternal management and outcome. Ultrasound Obstet Gynecol 2014; 44: 525–531.
Kohl T: Percutaneous minimally-invasive fetoscopic surgery for spina bifida aperta. I. Surgical technique and perioperative outcome. Ultrasound Obstet Gynecol 2014; 44: 515–524.
Higgins JPT, Altman DG, Gotzsche PC, Juni P, Moher D, Oxman AD, Savovic J, Schulz KF, Weeks L, Sterne JAC; Cochrane Bias Methods Group; Cochrane Statistical Methods Group: The Cochrane Collaboration’s tool for assessing risk of bias in randomised trials. BMJ 2011; 343:d5928.
National Institutes of Health: Study Quality Assessment Tools. Bethesda, National Institutes of Health, 2014.
Wells GA, Shea B, O’Connell D, Peterson J, Welch V, Losos M, Tugwell P: The Newcastle- Ottawa Scale (NOS) for assessing the quality of nonrandomised studies in meta-analyses; in Wells GA (ed): Clinical Epidemiology. Ottawa, Ottawa Hospital Research Institute, 2008.
Degenhardt J, Axt-Fliedner R, Enzensberger C, Tenzer A, Kawecki A, Kohl T: Peri- and postoperative management for minimally invasive fetoscopic surgery of spina bifida (in German). Z Geburtshilfe Neonatol 2014; 218: 244–247.
Bruner JP, Tulipan NE, Richards WO: Endoscopic coverage of fetal open myelomeningocele in utero. Am J Obstet Gynecol 1997; 176: 256–257.
Graf K, Wanis F, Neubauer BA, Kohl T, Uhl E, Kolodziej M: Neurosurgical follow-up after fetoscopic patch coverage of spina bifida; in 64th Annu Meet German Soc Neurosurg. Düsseldorf, German Medical Science GMS Publishing House, 2013.
Pedreira DA: Spina bifida: minimally invasive therapy; in 13th World Congr Fetal Med, Nice, 2014.
Graf K, Kohl T, Neubauer BA, Dey F, Faas D, Wanis FA, Reinges MH, Uhl E, Kolodziej M: Percutaneous minimally-invasive fetoscopic surgery for spina bifida aperta. III. Postnatal neurosurgical interventions in the first year of life. Ultrasound Obstet Gynecol 2015, Epub ahead of print.
Pedreira DA, Zanon N, de Sa RA, Acacio GL, Ogeda E, Belem TM, Chmait RH, Kontopoulos E, Quintero RA: Fetoscopic single-layer repair of open spina bifida using a cellulose patch: preliminary clinical experience. J Matern Fetal Neonatal Med 2014; 27: 1613–1619.
Pedreira DA, Zanon N, Nishikuni K, De Sa RA, Acacio GL, Chmait RH, Kontopoulos EV, Quintero RA: Endoscopic surgery for the antenatal treatment of myelomeningocele: the CECAM trial. Am J Obstet Gynecol 2016; 214: 111.e1–111.e11.
Grivell RM, Andersen C, Dodd JM: Prenatal versus postnatal repair procedures for spina bifida for improving infant and maternal outcomes. Cochrane Database Syst Rev 2014; CD008825.
Heuer GG, Adzick NS, Sutton LN: Fetal myelomeningocele closure: technical considerations. Fetal Diagn Ther 2015; 37: 166–171.
Pedreira DA, Valente PR, Abou-Jamra RC, Pelarigo CL, Silva LM, Goldenberg S: Successful fetal surgery for the repair of a ‘myelomeningocele- like’ defect created in the fetal rabbit. Fetal Diagn Ther 2003; 18: 201–206.
Pedreira DA, Sanchez e Oliveira Rde C, Valente PR, Abou-Jamra RC, Araujo A, Saldiva PH: Validation of the ovine fetus as an experimental model for the human myelomeningocele defect. Acta Cir Bras 2007; 22: 168–173.
Sanchez e Oliveira Rde C, Valente PR, Abou-Jamra RC, Araujo A, Saldiva PH, Pedreira DA: Biosynthetic cellulose induces the formation of a neoduramater following pre-natal correction of meningomyelocele in fetal sheep. Acta Cir Bras 2007; 22: 174–181.
Peeters SH, Van Zwet EW, Oepkes D, Lopriore E, Klumper FJ, Middeldorp JM: Learning curve for fetoscopic laser surgery using cumulative sum analysis. Acta Obstet Gynecol Scand 2014; 93: 705–711.
Moore MJ, Bennett CL: The learning curve for laparoscopic cholecystectomy. The southern surgeons club. Am J Surg 1995; 170: 55–59.
Kim JH, Lee IK, Kang WK, Oh ST, Kim JG, Lee YS: Initial experience of a surgical fellow in laparoscopic colorectal cancer surgery under training protocol and supervision: comparison of short-term results for 70 early cases (under supervision) and 73 late cases (without supervision). Surg Endosc 2013; 27: 2900–2906.
Claerhout F, Verguts J, Werbrouck E, Veldman J, Lewi P, Deprest J: Analysis of the learning process for laparoscopic sacrocolpopexy: identification of challenging steps. Int Urogynecol J 2014; 25: 1185–1191.
Claerhout F, Roovers JP, Lewi P, Verguts J, De Ridder D, Deprest J: Implementation of laparoscopic sacrocolpopexy – a single centre’s experience. Int Urogynecol J Pelvic Floor Dysfunct 2009; 20: 1119–1125.
Kohl T, Hartlage MG, Kiehitz D, Westphal M, Buller T, Achenbach S, Aryee S, Gembruch U, Brentrup A: Percutaneous fetoscopic patch coverage of experimental lumbosacral fullthickness skin lesions in sheep. Surg Endosc 2003; 17: 1218–1223.
American Association of Neurological Surgeons: Tethered Spinal Cord Syndrome. Rolling Meadows, American Association of Neurological Surgeons, 2014.
Kohl T: Presealing of chorioamniotic membranes prior to fetoscopic surgery disrupts the natural chorionic-uterine interface with unknown consequences. Eur J Obstet Gynecol Reprod Biol 2010; 148: 97–97.
Flake A: Percutaneous minimal-access fetoscopic surgery for myelomeningocele – not so minimal! Ultrasound Obstet Gynecol 2014; 44: 499–500.
Kohl T: Iatrogenic fetal membrane damage from complex fetoscopic surgery in human fetuses might not be amenable to simple closure by collagen plugs. Prenat Diagn 2008; 28: 876–877; author reply 878–880.
Beck V, Lewi P, Gucciardo L, Devlieger R: Preterm prelabor rupture of membranes and fetal survival after minimally invasive fetal surgery: a systematic review of the literature. Fetal Diagn Ther 2012; 31: 1–9.
Gratacos E, Sanin-Blair J, Lewi L, Toran N, Verbist G, Cabero L, Deprest J: A histological study of fetoscopic membrane defects to document membrane healing. Placenta 2006; 27: 452–456.
Engels AC, Van Calster B, Richter J, De- Koninck P, Lewi L, De Catte L, Devlieger R, Deprest JA: Collagen plug sealing of iatrogenic fetal membrane defects after fetoscopic surgery for congenital diaphragmatic hernia. Ultrasound Obstet Gynecol 2014; 43: 54–59.
Deprest JA, Evrard VA, Van Schoubroeck D, Vandenberghe K: Endoscopic cord ligation in selective feticide. Lancet 1996; 348: 890–891.
Wilson RD, Lemerand K, Johnson MP, Flake AW, Bebbington M, Hedrick HL, Adzick NS: Reproductive outcomes in subsequent pregnancies after a pregnancy complicated by open maternal-fetal surgery (1996–2007). Am J Obstet Gynecol 2010; 203: 209.e1–e6.
Farrell JA, Albanese CT, Jennings RW, Kilpatrick SJ, Bratton BJ, Harrison MR: Maternal fertility is not affected by fetal surgery. Fetal Diagn Ther 1999; 14: 190–192.
Meuli M, Meuli-Simmen C, Yingling CD, Hutchins GM, Hoffman KM, Harrison MR, Adzick NS: Creation of myelomeningocele in utero: a model of functional damage from spinal cord exposure in fetal sheep. J Pediatr Surg 1995; 30: 1028–1032; discussion 1032–1023.
Adzick NS: Fetal myelomeningocele: natural history, pathophysiology, and in-utero intervention. Semin Fetal Neonatal Med 2010; 15: 9–14.
Moher D, Liberati A, Tetzlaff J, Altman DG: Preferred reporting items for systematic reviews and meta-analyses: the PRISMA statement. PLoS Med 2009; 6:e1000097.